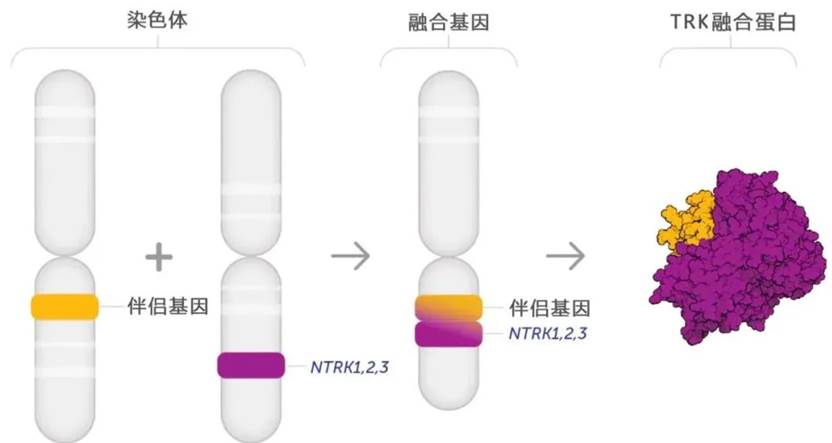
“钻石基因”NTRK:精准医疗的未来已来
NTRK基因家族的发现可追溯至1982年,由Mariano Barbacid课题组率先鉴定。该类基因编码一类神经营养因子受体,主要包括NTRK1、NTRK2和NTRK3三个亚型,分别对应产生TRKA、TRKB和TRKC蛋白。这些TRK激酶属于原肌球蛋白相关激酶家族,在神经组织中高度表达,对神经元的存活、生长以及功能维持具有核心调控作用。
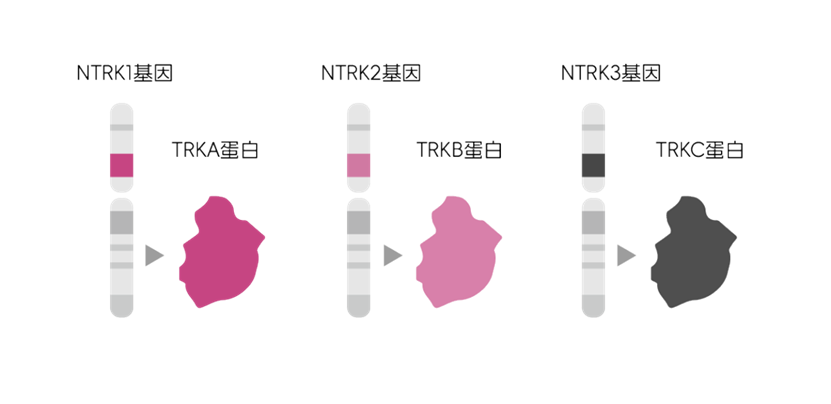
NTRK基因种类
一、NTRK的生理功能
其功能通过特异性配体-受体结合实现:神经生长因子(NGF)主要结合TRKA;脑源性神经营养因子(BDNF)及神经营养因子-4(NT-4)偏好结合TRKB;而神经营养因子-3(NT-3)虽可与三种TRK受体作用,但对TRKC亲和力最高。配体结合后激活下游关键信号通路——包括Ras/MAPK、PI3K及PLC-γ等,进而调控细胞生长、分化与存活。
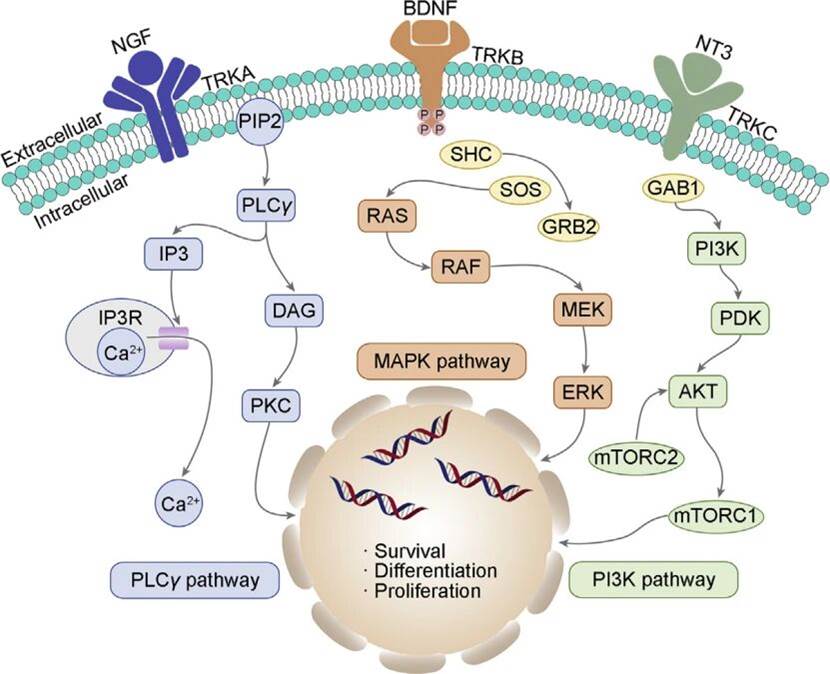
TRK激活后细胞内部的信号通路
TRK受体在中枢及外周神经系统中呈差异分布:TRKA集中于三叉神经节、背根神经节和胆碱能神经元,参与痛觉传导;TRKB广泛表达于多个脑区,调控情绪与食欲;TRKC则主要分布于中枢神经系统,与本体感觉的维持密切相关。此外,三类受体也在非神经组织中有表达,但其水平显著低于神经组织。
二、NTRK融合蛋白的致癌机制
深入研究揭示,NTRK基因除了在神经系统中发挥生理功能,其异常活化更是多种肿瘤发生发展的关键驱动因素。NTRK可通过基因突变、表达水平异常升高或基因融合等多种机制被激活,其中,尤以NTRK基因融合最为常见,也最具临床意义。
基因融合的具体过程(以NTRK1基因与TPM3基因融合为例)
这种致癌性融合通常发生在阅读框内,其后果是产生一种结构异常、功能失控的“嵌合蛋白”。该蛋白保留了TRK激酶结构域的完整活性,却因融合失去了原有的调控单元。其直接效应是:TRK激酶从受精密调控的“分子开关”转变为持续开启的“致癌引擎”。它不再依赖神经营养因子配体的结合,即可自主、高强度地激活下游多条关键信号通路(如RAS/MAPK、PI3K/AKT和JAK/STAT通路),从而不受控制地驱动肿瘤细胞的增殖、存活、侵袭与转移。
三、NTRK融合的癌种分布特征
NTRK基因融合在不同癌种中的分布呈现显著偏好性,其发生频率因肿瘤类型而异,体现出“癌种特异性”。从分子亚型来看,NTRK1和NTRK3融合较为多见,NTRK2融合则相对罕见。
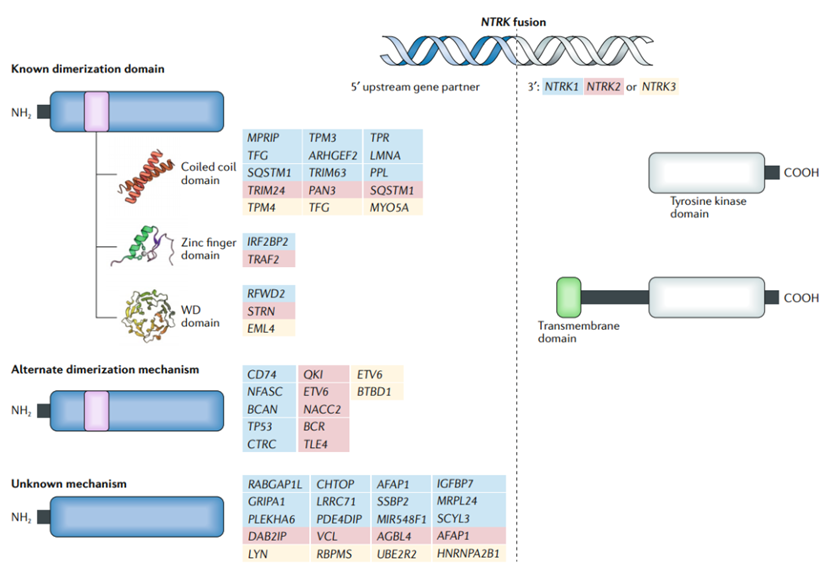
NTRK基因常见的融合的5′上游基因
在结构上,NTRK融合基因由5′端的伙伴基因(如ETV6、TPM3等)与3′端的NTRK激酶结构域(灰色表示)构成。不同伙伴基因(可使用颜色区分:NTRK1伙伴基因标蓝,NTRK2标红,NTRK3标黄)的参与,尤其是某些伙伴基因若引入跨膜区,可能影响融合蛋白在细胞中的定位与功能。
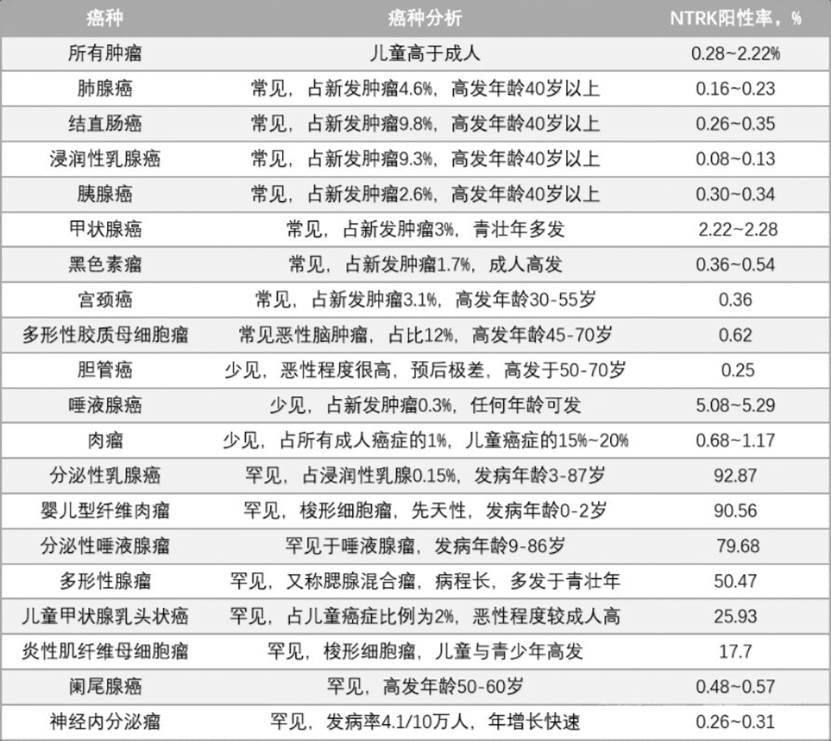
NTRK基因融合在不同癌症中发生频率各异
该融合事件在临床中呈现一个鲜明特征:“常见肿瘤不常见,罕见肿瘤很常见”。2021年发表于《NPJ Precision Oncology》的一项大宗研究(样本量>29.5万)显示,NTRK融合在全部恶性肿瘤中的总体检出率仅约0.30%。然而,在某些罕见肿瘤中,它却是关键的驱动因素,检出率可超过90%——如ETV6-NTRK3融合在分泌性乳腺癌、涎腺分泌性癌、先天性中胚层肾瘤及婴儿纤维肉瘤中具有极高发生率,已成为这类疾病的分子标志。也因此,ETV6-NTRK3成为目前认知最广泛的NTRK融合形式。
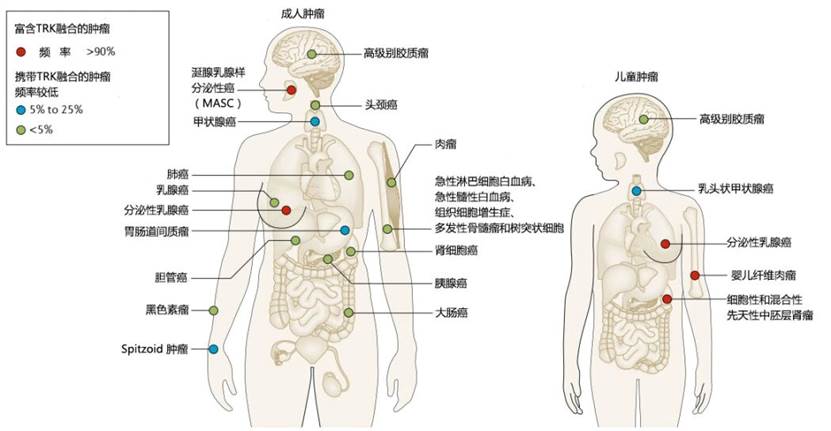
NTRK 融合在成人和儿童肿瘤中的分布和频率
基于这一独特的分布模式,目前国内外多项诊疗指南明确推荐,对成人分泌型乳腺癌、涎腺分泌样癌及婴儿纤维肉瘤患者常规进行NTRK基因检测,以实现精准靶向治疗。
四、攻克“钻石突变”:NTRK抑制剂的临床突破与未来
NTRK基因融合作为一种跨癌种存在的“广谱”靶点,已成为肿瘤精准治疗领域的热门研究方向。目前,全球已有两款特异性TRK抑制剂获批上市,为携带该突变的患者带来了革命性的治疗选择。
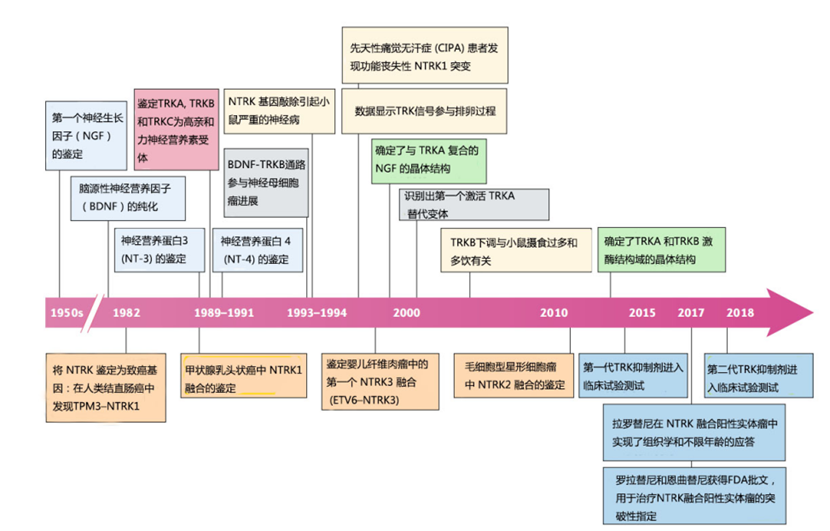
与 TRK 信号转导的生物学和治疗靶向相关的关键进展时间轴
首款“不限癌种”TRK抑制剂:拉罗替尼
拉罗替尼(Larotrectinib)作为首个获批的口服TRK抑制剂,适用于所有实体瘤类型,无需考虑肿瘤原发部位。其通过高选择性抑制TRK融合蛋白的活性,阻断下游致癌信号的传导,从而诱导肿瘤细胞凋亡并抑制生长。该药在分泌性乳腺癌、唾液腺癌和婴儿纤维肉瘤中显示出显著疗效。常见不良反应包括疲劳、恶心、呕吐、头晕等,亦可能引发转氨酶升高;少数患者可能出现发热、脱水等严重反应。该药具有胚胎-胎儿毒性,妊娠及哺乳期患者禁用。
拉罗替尼药品示意图
多靶点、强入脑:恩曲替尼
恩曲替尼(Entrectinib)是一种针对NTRK、ROS1和ALK融合的多靶点TKI药物。它通过竞争性结合激酶ATP位点,抑制激酶激活及下游信号通路,在多个癌种中表现出广谱抗肿瘤活性。与拉罗替尼相比,恩曲替尼不仅能抑制更多靶点,还可有效穿透血脑屏障,对颅内转移灶控制尤为出色,临床研究显示其颅内缓解率接近100%。其适应症覆盖乳腺癌、 NSCLC、肉瘤、甲状腺癌等多种实体瘤。常见不良事件包括疲劳、便秘、水肿、头晕等,总体安全性可控。

恩曲替尼药品示意图
国内上市与未来展望
拉罗替尼和恩曲替尼均于2022年在中国获批上市,不仅强化了NTRK“钻石基因”的临床地位,也标志着我国肿瘤诊疗正式迈进“生物标志物驱动”的精准时代。此外,新一代TRK抑制剂如瑞波替尼(Repotrectinib)和他雷替尼(Taletrectinib)等在研药物已展示出卓越的临床潜力,尤其对获得性耐药突变具有抑制效果。未来,随着更多创新药物的涌现,NTRK靶点治疗领域有望迎来更广阔的应用前景。
🎯探索最新治疗机会: 除了已上市的药物,全球范围内仍有大量针对NTRK融合的创新疗法和联合用药的临床试验正在招募患者。如果您想了解自己是否符合这些前沿治疗的入组条件,可以通过专业平台https://www.trialsfinder.net/查询最新的NTRK相关临床试验信息,寻找可能受益的创新治疗机会。